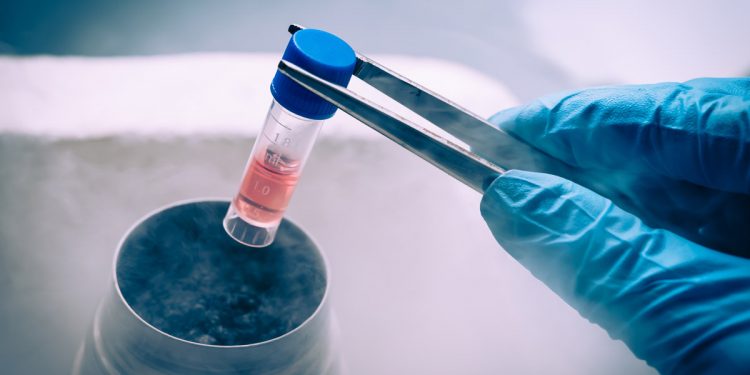
Sclerosi multipla: si è concluso il trial clinico di Fase I con trapianto di staminali cerebrali. Un traguardo che accende nuove speranze per il trattamento di questa malattia neurodegenerativa. Per la prima volta al mondo sono stati trattati tutti i pazienti reclutati in una sperimentazione con trapianto di cellule staminali cerebrali per il trattamento sperimentale della Sclerosi Multipla Secondaria Progressiva. E nessuno ha mostrato effetti collaterali, né subito dopo il trapianto, né nei mesi successivi.
A dare l’annuncio è stata la Pontificia Accademia per la Vita, insieme all’Associazione Revert Onlus e alla Fondazione Casa Sollievo della Sofferenza, Opera di San Pio da Pietrelcina l, che hanno coordinato e finanziato la sperimentazione.
L’occasione è la Giornata mondiale sulla Sclerosi Multipla, che si celebra il 30 maggio e che quest’anno festeggia questo importante successo. Si tratta del primo passo verso lo sviluppo di un protocollo sperimentale per trattare i pazienti affetti da sclerosi multipla con il trapianto di cellule staminali cerebrali umane di grado clinico.
Cellule staminali cerebrali contro la sclerosi multipla: la sperimentazione
La sperimentazione di Fase I è iniziata a gennaio 2018 con il ricovero del primo paziente. Il suo obiettivo è verificare la sicurezza del trattamento e le possibili azioni neurologiche. I quindici pazienti previsti nel protocollo sono stati suddivisi in quattro gruppi e trapiantati con dosi crescenti di cellule. Gli ultimi sei hanno ricevuto il dosaggio più elevato, pari a 24 milioni di cellule. Non si sono verificati effetti collaterali, né dopo il trapianto, né nei mesi successivi. Le équipe cliniche proseguiranno l’attività di monitoraggio per almeno un anno dopo l’intervento e sono attualmente impegnate nella valutazione degli eventuali effetti terapeutici.
“Siamo felici di annunciare questo importante traguardo nella sperimentazione in corso con cellule staminali cerebrali”. Lo ha detto Angelo Vescovi, Direttore Scientifico dell’IRCCS Casa Sollievo della Sofferenza di San Giovanni Rotondo e presidente dell’Advisory Board di Revert Onlus, nonché Professore dell’Università degli Studi di Milano Bicocca. “Aspettiamo adesso il follow-up a un anno e la sottomissione nei tempi più brevi possibili del protocollo per la Fase II”.
La sperimentazione è basata su dati scientifici pubblicati nel 2003 sulla rivista Nature. Questo studio clinico di Fase I per la Sclerosi Multipla rappresenta la terza tappa di un percorso iniziato 12 anni fa con la creazione della banca mondiale di staminali del cervello umano, ancora oggi unica al mondo.
Lo studio è proseguito con il primo trapianto in diciotto pazienti con SLA nel 2012.
La sperimentazione è stata coordinata e finanziata dalla Fondazione e dall’IRCCS Casa Sollievo della Sofferenza e da Revert Onlus con il patrocinio della Fondazione Cellule Staminali di Terni. Hanno collaborato l’Azienda Ospedaliera di Terni, l’Università di Milano Bicocca e l’Ospedale Cantonale di Lugano.
Sclerosi multipla: cos’è
La sclerosi multipla è una malattia cronica neurodegenerativa che colpisce il sistema nervoso centrale, con conseguenze anche altamente invalidanti. Si tratta di una patologia autoimmune. E’ infatti caratterizzata da una reazione anomala delle difese immunitarie, che attaccano alcuni componenti del sistema nervoso centrale scambiandoli per agenti estranei. Ad essere danneggiata è la mielina, ovvero la guaina che circonda le fibre nervose.
Ad oggi non esiste una cura definitiva, ma molte terapie sono in grado di rallentare la progressione della malattia, migliorando i sintomi e la qualità della vita. Questa sperimentazione rappresenta quindi un traguardo importantissimo per dare una speranza in più a chi soffre di sclerosi multipla e altre malattie neurologiche. Se vuoi saperne di più su questa patologia, leggi il nostro articolo “Sclerosi multipla: che cos’è, sintomi, diagnosi e cura”.
Puoi approfondire i dettagli della sperimentazione sul sito della Pontificia Accademia per la Vita.
Ti è piaciuto questo articolo? Condividilo su Pinterest.