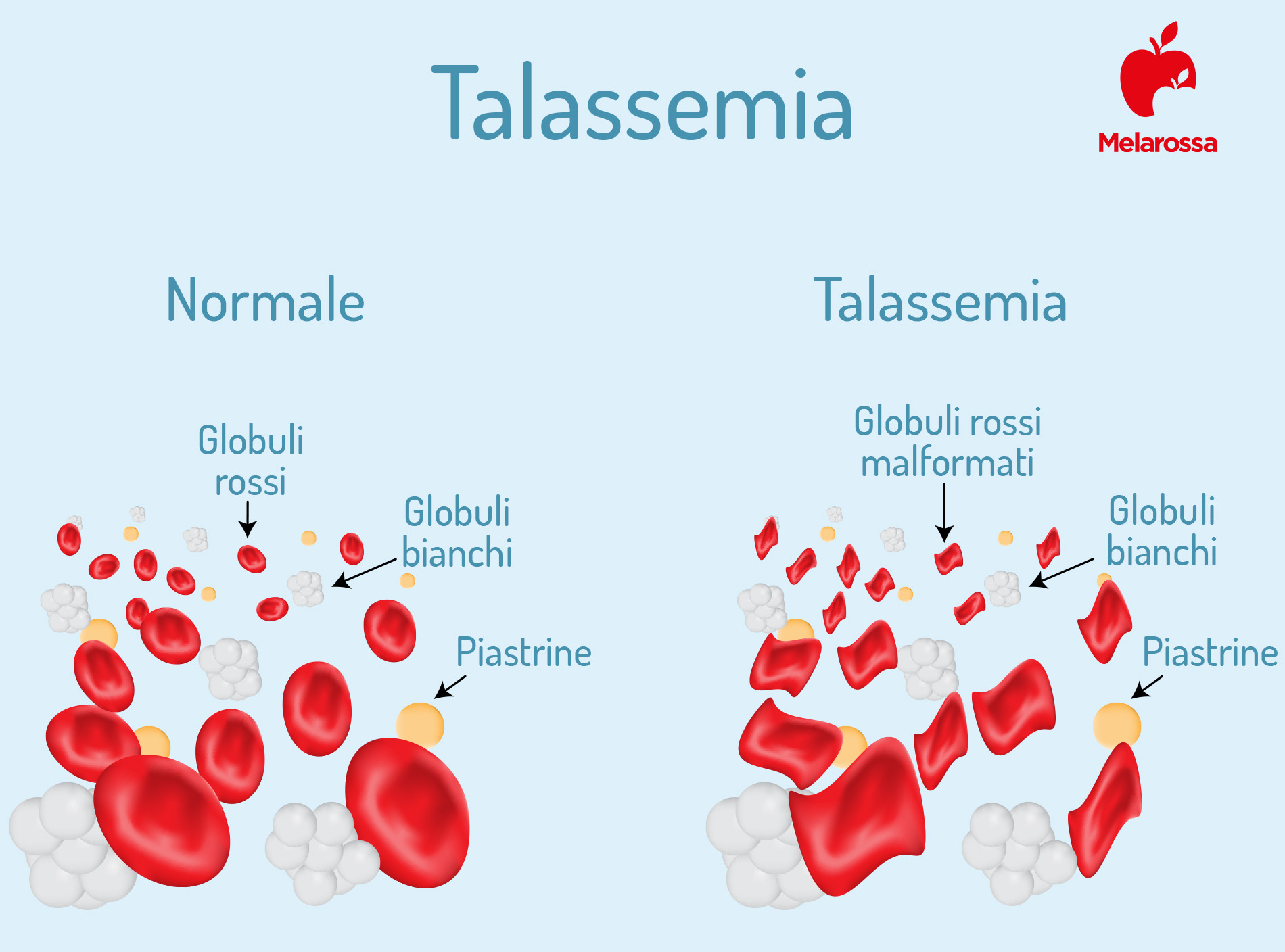
L’anemia mediterranea o talassemia è un termine usato per indicare un gruppo di disturbi caratterizzati da ridotti livelli di emoglobina, di produzione di globuli rossi e anemia.
Ne esistono due forme principali: alfa talassemia e beta talassemia, ciascuna con vari sottotipi. La beta talassemia major è stata descritta per la prima volta nella letteratura medica nel 1925 da un medico americano, Thomas Cooley, per cui è anche conosciuta come anemia di Cooley.
La patologia colpisce un individuo su 100.000, con una frequenza maggiore nelle popolazioni mediterranee, incluso il nord Africa ed il Medio Oriente. In Italia è più comune nella regione Sardegna.
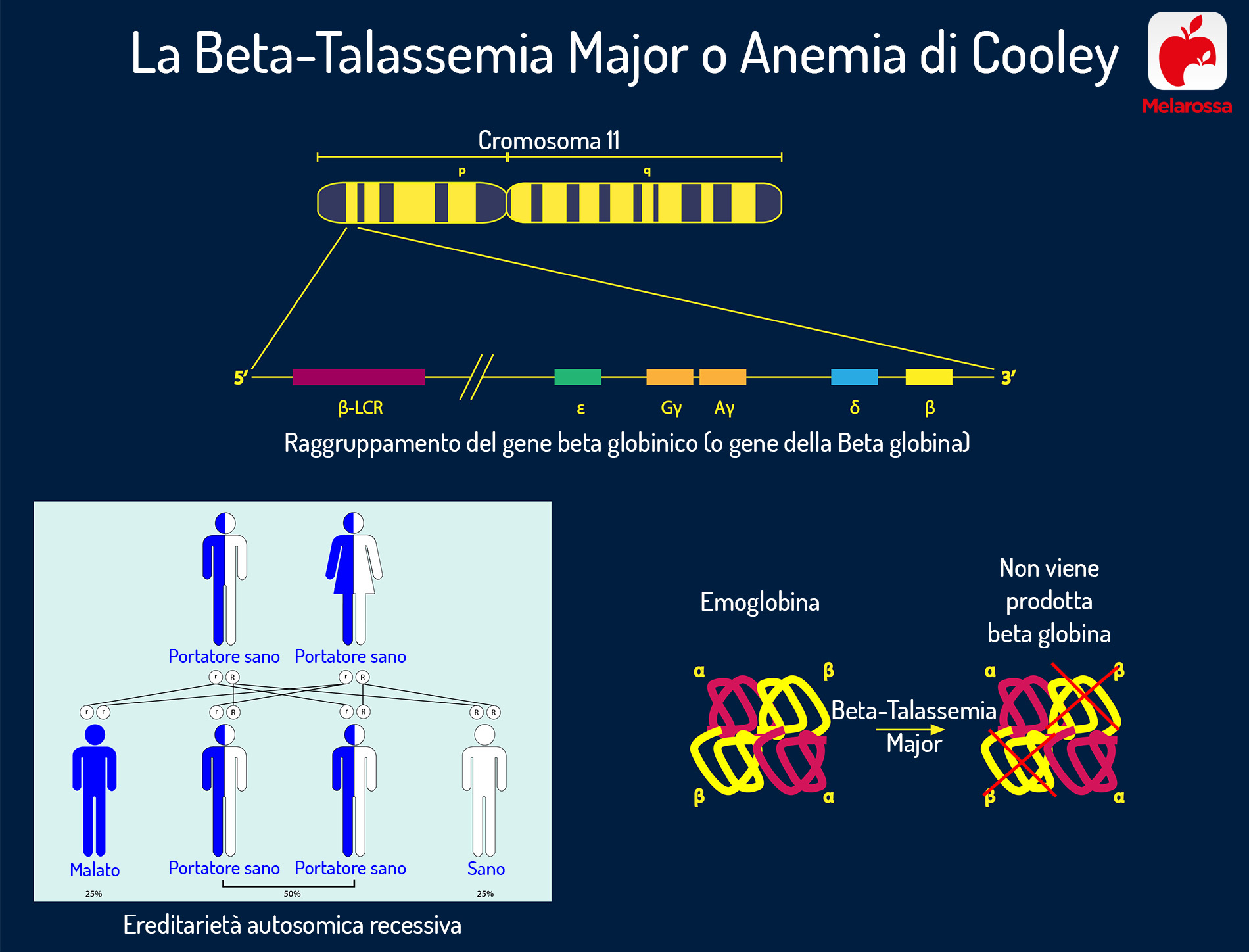
E’ causata da una mutazione del cromosoma 11 e la patologia è autosomica recessiva. Oggi, il classico quadro clinico della beta talassemia major si osserva principalmente in Paesi con risorse insufficienti per fornire un trattamento alle persone affette (trasfusioni regolari e farmaci per abbassare il ferro ematico).
La prognosi dell’anemia mediterranea varia molto da caso a caso ed è maggiormente influenzata dai depositi di ferro in eccesso dovuti a continue trasfusioni (i farmaci chelanti prevengono ciò).
La cura definitiva avviene solo in caso di trapianto, ma la ricerca sta facendo progressi nel campo della terapia genica.
Anemia mediterranea: che cos’è
Nota come beta-talassemia major o anemia di Cooley (dal medico che la scoprì nel 1925), è una patologia ereditaria caratterizzata da globuli rossi più piccoli (microcitemia).
L’emoglobina si trova nei globuli rossi di bambini e adulti ed è formata da due catene alfa e due beta.
Essa ricopre un ruolo chiave nel trasporto dell’ossigeno. Resistente ai trattamenti usuali per la carenza di ferro, l’anemia mediterranea è dovuta a difetti nella produzione delle catene beta, che vengono sostituite da due catene delta, provocando la comparsa di anemia microcitica (con globuli rossi più piccoli del normale) e scarsa ossigenazione dei tessuti.
Inoltre, a causa della produzione difettosa di catene beta, le alfa si uniscono e formano degli aggregati che danneggiano la membrana del globulo rosso. Ne deriva la distruzione precoce degli eritrociti nel midollo e, in misura minore, nella milza.
Epidemiologia
La beta-talassemia ha un’incidenza complessiva di circa 1 persona su 100.000 con una frequenza maggiore nelle popolazioni mediterranee.
ll nome deriva dalla diffusione nelle aree che si affacciano sul bacino del mar Mediterraneo, incluso il nord Africa ed il Medio Oriente. In Italia la maggior incidenza si riscontra in Sardegna.
Questa forma di anemia è anche chiamata beta-talassemia perché determinata dalla mutazione dei geni che controllano la produzione di una delle catene beta che costituiscono l’emoglobina, il mezzo di trasporto dell’ossigeno nel sangue.
Se ti interessa l’argomento, scopri tutto su i tipi di anemia.
Quali sono le cause dell’anemia mediterranea
L’anemia mediterranea è una malattia ematologica ereditaria, trasmessa da genitore a figlio e causata da una mutazione nel gene HBB sul cromosoma 11.
La patologia è autosomica recessiva, quindi entrambi i genitori devono essere portatori del gene patologico per trasmetterlo alla prole. La gravità della malattia dipende dalla natura della mutazione.
Portatore sano di talassemia
Un portatore sano di anemia mediterranea è un soggetto il quale presenta nel proprio patrimonio genetico una mutazione, che però non si è mai manifestata come malattia.
Chiunque può essere portatore di talassemia, ma è molto più comune nelle persone di determinate origini etniche o che hanno familiari originari del:
- bacino del Mediterraneo tra cui Italia, Grecia e Cipro.
- India, Pakistan e Bangladesh.
- Medio Oriente.
- Cina e sud-est asiatico.
Basta un semplice esame del sangue per confermare che si è portatori, se si pensa di essere a rischio.
Classificazione
Esistono diversi tipi di talassemia:
1: ß Talassemia minor: è un difetto genetico che si presenta come una leggera anemia. I soggetti sono persone che di solito non necessitano di cure, ma solo di regolari visite di controllo e possono essere identificate solo da specifici esami ematologici.
2: Talassemia intermedia: può avere aspetti diversi, da asintomatica, simile alla talassemia minor, a grave, dove il soggetto diventa dipendente dalle trasfusioni di sangue.
3: Talassemia major (anemia di Cooley): è associata a un’anemia emolitica estremamente grave dipendente da trasfusioni di sangue per tutta la vita. Si manifesta nei primi mesi o nei primi anni con una grave amenità, pallore della pelle, scarso sviluppo statura-peso ed epatosplenomegalia.
Trasmissione ai figli
La talassemia si verifica quando uno o entrambi i geni che producono la beta globina non funzionano o funzionano solo parzialmente. L’essere umano ha bisogno di entrambe le catene, alfa e beta, per formare l’emoglobina.
Se il soggetto ha una predisposizione genetica e solo uno dei geni colpiti, presenta una lieve anemia e di solito non ha bisogno di cure. Se invece entrambi i geni della globina sono colpiti, il paziente ha una grave anemia poiché ha ereditato da entrambi i genitori (talassemia major).
I sintomi di questo tipo di anemia compaiono nei primi sei mesi di vita e il trattamento consiste nell’eseguire trasfusioni di sangue, ad intervalli regolari, a 14-21 giorni. Se le trasfusioni iniziano in tenera età e continuano per tutta la vita, la prognosi è favorevole.
A causa di questo trattamento però, il paziente accumula nell’organismo depositi di ferro che richiedono un trattamento con farmaci ferrochelanti che possono essere somministrati per via orale o tramite microperfusioni quotidiane, cutanee, prolungate per 12 ore o utilizzando una pompa per iniezione.
Fattori di rischio
I fattori di rischio per la beta-talassemia sono esclusivamente genetici, essendo determinati da mutazioni nel gene HBB che codifica per la catena beta della globina.
Le mutazioni sono ereditate in modo autosomico recessivo, il che significa che per essere colpita, una persona deve prendere un gene malato da ciascun genitore.
Le forme della malattia sono correlate al numero di geni patologici ricevuti.
L’individuo può avere solo una copia del gene interessato, che causa una beta-talassemia minor. In caso di entrambi i geni affetti, può svilupparsi una beta-talassemia intermedia o major.

Quali sono i sintomi dell’anemia mediterranea?
L’anemia mediterranea presenta immagini cliniche molto variabili che dipendono dalla gravità dell’aberrazione genetica sottostante.
Le forme lievi di questo disturbo ematologico possono essere quasi asintomatiche. In altri casi invece, specialmente nell’anemia mediterranea major, i sintomi possono includere:
- pallore
- Affaticamento.
- Debolezza muscolare.
- Sviluppo lento e ittero nei bambini.
- Alterazioni ossee (ispessimento del cranio, zigomi prominenti, ginocchio valgo e fratture patologiche delle ossa lunghe).
- Anoressia (mancanza di appetito).
- Attacchi di febbre ricorrenti.
- Diarrea.
- Irritabilità.
- Distensione progressiva dell’addome (secondaria a splenomegalia ed epatomegalia).
Nel caso di trasfusioni regolari, la crescita e lo sviluppo del bambino affetto da anemia mediterranea tendono ad essere normali.
Ma, nel tempo, possono verificarsi complicazioni da sovraccarico di ferro, come lo sviluppo tardivo del corpo e della maturazione sessuale, emocromatosi e fibrosi epatica.
Inoltre, per compensare la mancanza di globuli rossi, il midollo osseo si sforza di produrne di più e questa reazione si traduce nella tendenza a formare ossa più lunghe e fragili, con rischio di osteoporosi. Meccanismo simile è nella milza, ugualmente sollecitata.
Le conseguenze sono un allargamento dell’organo, che, inoltre, viene distratto da altre funzioni come aiutare a difendere l’organismo dalle infezioni. La frequenza delle trasfusioni di sangue, dovuta al trattamento dell’anemia mediterranea grave, crea un accumulo di ferro, con il rischio di danneggiare altri organi come fegato e cuore.
Tra le altre conseguenze dell’anemia mediterranea possiamo ritrovare:
- disturbi endocrini e squilibri ormonali (inclusi ipotiroidismo, insufficienza paratiroidea, surrenalica e diabete).
- Colelitiasi (come nell’anemia falciforme).
- Ulcere cutanee degli arti inferiori dovute a insufficienza venosa cronica.
Le persone con anemia mediterranea sono, allo stesso tempo, maggiormente protette dalla malaria poiché i globuli rossi sono piccoli e il Plasmodium non può sfruttare il sistema sanguigno che vorrebbe parassitare.

Diagnosi dell’anemia mediterranea
La diagnosi di laboratorio comprende l’esecuzione di:
- Emocromo completo, che fornisce dati sul numero di eritrociti, la loro dimensione (MCV) e la quantità di emoglobina (MCH, entrambi bassi).
- Striscio di sangue periferico.
- Elettroforesi per misurare Hb A e Hb A2, componenti dell’emoglobina adulta.
- Test genetici: se i dati non chiariscono la diagnosi si esegue un test del DNA; per un quadro completo a volte è necessario indagare sui familiari.
- Capacità di legare il ferro.
- Dosaggio dell’emopessina.
Tutti i pazienti con talassemia dovrebbero indagare sui loro fratelli, genitori, e parenti stretti al fine di diagnosticare i portatori asintomatici.
Anche l’indagine dei partner deve essere fatta prima di un’eventuale gravidanza, seguita, in caso, da una consulenza genetica.
Le coppie a rischio (entrambi i partner con talassemia minor) dovrebbero essere avvertite che esiste una possibilità del 25% di avere un figlio con talassemia major, del 50% portatore sano e del 25% sano.
La diagnosi di talassemia major viene generalmente posta nei primi mesi di vita, il più delle volte al di sotto dei 2 anni. La diagnosi molecolare è utile per identificare mutazioni correlabili con la gravità.

Diagnosi prenatale
La diagnosi genetica prenatale, a seconda dell’età gestazionale, può essere effettuata tramite:
- Biopsia dei villi coriali: nella 10-12 settimana di gravidanza.
- Amniocentesi: nel secondo trimestre, sotto guida ecografica, viene inserito un ago attraverso l’addome della madre e viene aspirata una piccola quantità di liquido amniotico, che contiene anche cellule fetali che vengono analizzate geneticamente.
- Cordonocentesi: dopo la 18° settimana di gravidanza si inserisce un ago nel cordone ombelicale, sotto guida ecografica, e si aspira una piccola quantità di sangue fetale.
Trattamento
La trasfusione di sangue è il trattamento di base nella talassemia major. Il regime inizia nei primi anni di vita, dalla diagnosi, e viene eseguito ad intervalli regolari di 2-6 settimane.
Come risultato di queste trasfusioni ripetute, nel corpo si accumulano grandi quantità di ferro, che viene immagazzinato principalmente in:
- fegato.
- Pancreas.
- Milza.
- Cuore.
- Ghiandole endocrine.
- Pelle.
Poiché il corpo non dispone di meccanismi propri per eliminare questo elemento in eccesso e poiché sviluppa anche meccanismi compensatori per l’assorbimento eccessivo, è stato stabilito un regime di terapia con farmaci chelanti.
Essi si legano al ferro (con una reazione chimica simile a due chele) e ne favoriscono l’eliminazione.
La sopravvivenza a lungo termine dei pazienti con talassemia major dipende dall’efficacia di questo trattamento.
L’unica terapia in grado di fornire una cura definitiva è il trapianto di midollo osseo, in particolare l’allotrapianto (con cellule ematopoietiche da un fratello o da un donatore non imparentato).
A questo scopo possono essere utilizzate:
- Cellule emopoietiche da un fratello (donazione fraterna).
- Sangue del cordone ombelicale/cellule embrionali.
- Cellule ematopoietiche da un donatore non imparentato.
Prognosi e decorso dell’anemia mediterranea
Poiché la talassemia è una malattia genetica, non c’è modo di prevenirla. Tuttavia è possibile gestirla per evitarne le complicazioni.
Oltre a una dieta sana, un regolare esercizio fisico può aiutare i sintomi e la prognosi. Di solito si consigliano allenamenti di intensità moderata come camminare e andare in bicicletta.
Anche il nuoto e lo yoga sono raccomandati e fanno bene anche alle articolazioni. L’importante è trovare qualcosa che piaccia per rimanere in movimento.
Aspettativa di vita
La talassemia è una malattia grave che può portare a complicazioni potenzialmente letali se non trattata.
Sebbene sia difficile individuare un’esatta aspettativa di vita, la regola generale è che più grave è la condizione, più rapidamente può diventare fatale.
Una cattiva prognosi può avere a che fare con il sovraccarico di ferro, che alla fine può arrivare a colpire gli organi interni.
Prima viene diagnosticata la talassemia e prima si può ricevere trattamento.
I ricercatori stanno continuando a esplorare i test genetici e la possibilità della terapia genica; in futuro questa potrebbe riattivare l’emoglobina e disattivare le mutazioni anomale nel DNA.

Anemia mediterranea: cosa mangiare e cosa evitare
Una dieta equilibrata, ricca di verdura e frutta, rispettando i tre pasti principali al giorno, aiuta a mantenere l’organismo sano.
Le cause più note che portano alle complicazioni dell’anemia mediterranea possono essere problemi al fegato, problemi cardiaci, ed altri dovuti al sovraccarico di ferro a seguito di regolari trasfusioni di sangue.
Al fine di prevenire e ridurre il più possibile questo sovraccarico, oltre all’utilizzo dei farmaci chelanti, si consiglia una dieta con alimenti a basso contenuto di ferro.
Consumo moderato
Gli alimenti che contengono una grande quantità di ferro includono:
- fegato.
- Manzo.
- Fagioli.
- Maiale.
- Arachidi.
- Tofu.
Inoltre vanno evitati:
- prugne.
- Spinaci.
- Piselli.
- Broccoli.
- Melone.
- Verdure a foglia verde.
Invece, si raccomanda di consumare cibi ricchi di acido folico, calcio e vitamina D come salmone, tonno, alici, latte di mucca e di soia.
Possono essere presi in considerazione anche gli integratori alimentari degli stessi elementi inclusa la vitamina B6, sotto controllo dello specialista.
Fonti
- Giambona A, Passarello C, Vinciguerra M, Li Muli R, Teresi P, Anzà M, Ruggeri G, Renda D, Maggio A. Significance of borderline hemoglobin A2 values in an Italian population with a high prevalence of beta-thalassemia. Haematologica. 2008 Sep;93(9):1380-4. doi: 10.3324/haematol.12840. Epub 2008 Jul 4. PMID: 18603555.
- Cardiero G, Musollino G, Friscia MG, Testa R, Virruso L, Di Girgenti C, Caldora M, Colella Bisogno R, Gaudiano C, Manco G, Lacerra G. Effect of Mutations on mRNA and Globin Stability: The Cases of Hb Bernalda/Groene Hart and Hb Southern Italy. Genes (Basel). 2020 Jul 31;11(8):870. doi: 10.3390/genes11080870. PMID: 32751969; PMCID: PMC7466077.
- Karimi M, Cohan N, De Sanctis V, Mallat NS, Taher A. Guidelines for diagnosis and management of Beta-thalassemia intermedia. Pediatr Hematol Oncol. 2014 Oct;31(7):583-96. doi: 10.3109/08880018.2014.937884. PMID: 25247665.
- Perrimond H. beta-thalassémie–manifestations cliniques [Beta-thalassemia: clinical manifestations]. Bull Soc Pathol Exot. 2001 May;94(2):92-4. French. PMID: 11475035.
Ti è piaciuto il nostro articolo? Condividilo su Pinterest.